Cáncer de vejiga
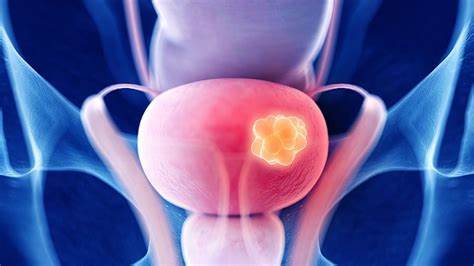
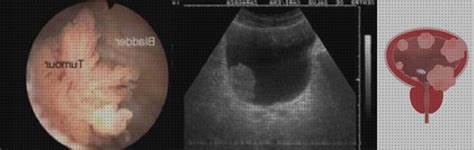
El cáncer de vejiga o cáncer vesical es un tipo de tumor maligno que aparece en la vejiga urinaria. Los principales factores para el desarrollo del cáncer de vejiga incluyen productos químicos específicos, que se encuentran fundamentalmente en el humo de los cigarrillos. En los países del Tercer Mundo, ciertas infecciones parasitarias. El tratamiento del cáncer vesical gira en función de la extensión del mismo, generalmente se resuelve con quimioterapia, la remoción de la vejiga o la quimioterapia sistémica. Se distinguen el cáncer superficial de vejiga del cáncer invasivo. Si el cáncer sigue siendo superficial, suele cursar con un buen pronóstico, mientras que el cáncer invasivo de la vejiga es mucho más grave y requiere tratamiento agresivo. Cuando la enfermedad se asocia con la amplia presencia de metástasis ya no es posible la curación del paciente.
El interior de la vejiga está revestido con las células de transición que son responsables de la mayoría de los cánceres de la vejiga. La progresión depende en gran medida de la agresividad del tumor. La edad avanzada y las enfermedades coexistentes se asocian a tasas más altas de mortalidad por cualquier causa.
La incidencia del cáncer de vejiga está aumentando en los países occidentales. En 1996, aproximadamente 53 000 personas fueron diagnosticadas de cáncer de vejiga en los Estados Unidos, 9000 en Francia, 2000 en Suecia, 8000 en España y 1200 en Bélgica.
Los tumores vesicales constituyen el 10 % de los tumores del varón. Afectan predominantemente a los hombres (relación 4:1 con las mujeres).
El cáncer de la vejiga ocupa el sexto lugar entre las neoplasias malignas más frecuentes en Estados Unidos de América (EUA), en 2013 se estimaron 72 570 casos nuevos diagnosticados y 15.210 muertes.
Aproximadamente el 75-85 % de los pacientes presentan el cáncer confinado en la mucosa (estadio Ta-Tis) o submucosa (estadio T1). El otro 15-25 % de los pacientes presentan invasión de la capa muscular o afectación de los ganglios linfáticos pélvicos (estadio T2-T4, N+). El manejo del cáncer superficial de vejiga tiende a ser más complejo debido a diferentes opiniones entre los urólogos.
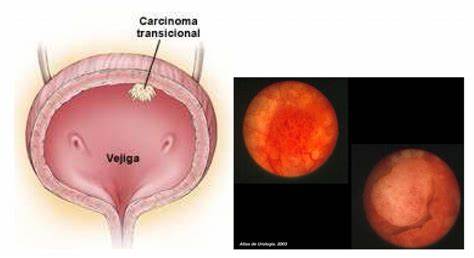
La mayor parte de los tumores de vejiga (60 %) se localizan en el trígono vesical. Más del 90 % de los tumores vesicales son carcinomas de células transicionales. El resto son carcinomas escamosos o adenocarcinomas.
Los factores más importantes, para la aparición de un carcinoma de vejiga, son el tabaco y ciertos productos químicos cancerígenos, de tal manera que bajo ciertas circunstancias puede ser considerada como una enfermedad profesional. El riesgo de cáncer de vejiga también aumenta significativamente con la edad. Las principales industrias de las sustancias carcinogénicas en cuestión son:
El tabaco es otro importante factor de riesgo porque está asociado a una alta mortalidad por cáncer de vejiga durante largo seguimiento de fumadores. Incluso el pronóstico de los fumadores es peor que otros factores, como el estadio, grado histológico, tamaño o multifocalidad del tumor. Los pacientes que inicialmente tienen un grado histológico G3 en el tumor, son más a menudo grandes fumadores que los que tienen tumores menos agresivos. Un estudio español ha demostrado que mientras que los fumadores/as de tabaco rubio, al cabo de 10 años de dejar de fumar tienen un riesgo parecido al de los no fumadores/as de su edad, los fumadores/as de tabaco negro tienen un aumento de riesgo de cáncer de vejiga que permanece toda la vida, aunque dejen de fumar. También existe aumento de riesgo en algunas ocupaciones, como la imprenta y la peluquería.
Las lesiones por la esquistosomiasis urinaria pueden degenerar en lesiones malignas, como el carcinoma de células escamosas de la vejiga. Esta enfermedad se da principalmente en Egipto y África occidental.
También se encuentran en el origen del cáncer de vejiga algunos fármacos (fenacetina, ciclofosfamida), la radiación pélvica y el consumo elevado de café. En la región de la Península Balcánica, se ha instalado un cáncer urotelial endémico, una enfermedad que resulta por intoxicación alimentaria con la micotoxina, ocratoxina A, producida por un hongo de los cereales.
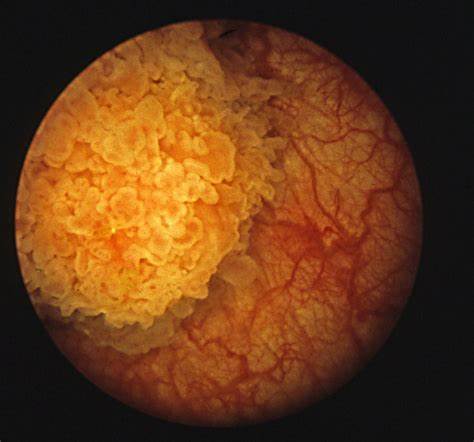
Al igual que todos los cánceres, el desarrollo de cáncer de la vejiga implica la adquisición de varias mutaciones en oncogenes y genes supresores de tumores. Los genes que pueden ser alterados en el cáncer de la vejiga incluyen FGFR3, HRAS, RB1 y TP53. Así pues, los antecedentes familiares de cáncer de la vejiga son también un factor de riesgo para la enfermedad. Se cree que algunas personas aparentemente heredan una disminución de la capacidad para romper algunas sustancias químicas, lo que las hace más sensibles a los efectos
La clasificación TNM (tumor, ganglios linfáticos-nodos y metástasis) de la Unión Internacional contra el Cáncer de 2003 es la más aceptada:
Los carcinomas de imagen pueden ser clasificados por diferentes métodos como: cistoscopia, resección transuretral, estudio de imagen como ecografía, TAC o RMN o estudios histopatológicos obtenidos de la cirugía.
Según esta clasificación del tumor primario, los tumores de vejiga se clasifican en dos grandes grupos:
El grado histológico de la OMS es la clasificación generalmente más aplicada en todo el mundo, siendo G el grado histológico de diferenciación.
La hematuria es el síntoma más frecuente en el cáncer de vejiga. El grado de hematuria no se correlaciona con la extensión de la enfermedad. Puede ser una hematuria macroscópica, franca o visible por el propio paciente o detectada en un análisis de orina. Cualquier grado de hematuria, sin embargo, requiere descartar un cáncer de vejiga, incluso si existen otras posibles causas de hematuria, como los cálculos urinarios, cistitis bacterianas, etc.
El cáncer de vejiga también puede presentarse como un síndrome miccional, indicativo de irritación vesical. Los pacientes pueden quejarse de urgencia miccional, disuria y aumento de la frecuencia miccional (polaquiuria). Aunque estos síntomas son más indicativos de cistitis bacteriana, los cultivos bacterianos negativos con una persistencia de los síntomas, con o sin hematuria, deben investigarse con rapidez para descartar la posible presencia de un cáncer de vejiga, incluido un carcinoma in situ (CIS).
La búsqueda sistemática de hematuria microscópica asintomática no es una prueba clara, excepto en pacientes de más de 50 años que deben ser examinados por un urólogo. La incidencia de tumores ocultos en pacientes de más de 50 años con hematuria microscópica asintomática es del 5 % aproximadamente, cuando la incidencia es de alrededor del 10 % si se detecta una hematuria microscópica sintomática.
El cribado de la hematuria asintomática no se recomienda porque el valor predictivo positivo es muy bajo (0,5 %) para recomendar la búsqueda de masas vesicales. Sin embargo, el cribado sistemático para detectar hematuria microscópica puede estar indicado en poblaciones expuestas a carcinógenos vesicales, incluidos los fumadores.
El reconocimiento precoz de los tumores de vejiga está asociado a un mejor pronóstico. Un programa educacional diseñado para la población general y para los médicos de atención primaria es crucial para promover un diagnóstico precoz, incluyendo la detección en pacientes asintomáticos mayores de 45 años.
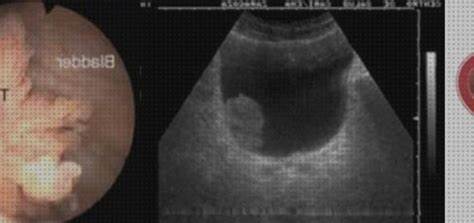
Dado que la mayoría de los carcinomas cursan con hematuria, el cáncer de vejiga debe ser excluido como causa de este síntoma. En algunos casos se ha identificado un tumor vesical con un examen de ultrasonido de los riñones y la vejiga. Del mismo modo, se ha valido de una urografía con contraste intravenoso para diagnosticar un carcinoma de vejiga. Una tomografía computarizada (TC) puede revelar el tumor.
Sin embargo, la exploración cistoscópica con toma de biopsias profundas de las zonas alteradas es imprescindible para realizar el diagnóstico y seguir la evolución del cáncer vesical. La citología de orina es una prueba que suele hacerse antes de la cistoscopía y la biopsia, en la que se tiñe la superficie de las células en la orina y se detecta microscópicamente las que son malignas, con una sensibilidad de aproximadamente 80-90 %. Para tumores bien diferenciados, la posibilidad de que las células cancerosas sean descubiertos no suele ser satisfactoria.
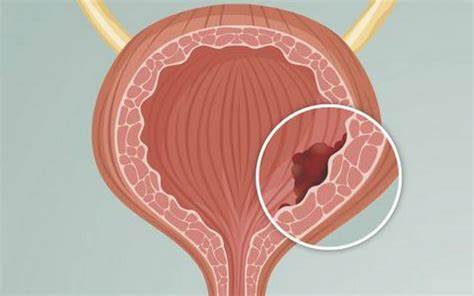
Los marcadores tumorales han estado recientemente disponibles, los cuales tienen una sensibilidad superior a la urocitología tradicional, pero una menor especificidad. Por lo tanto, pueden mejorar la probabilidad de detectar la enfermedad en una fase temprana.
El diagnóstico definitivo se realiza en la resección del tumor, como parte de un examen histológico. Después del diagnóstico, se indica la búsqueda de metástasis. Los carcinomas de vejiga se diseminan a través del torrente sanguíneo más comúnmente hacia los pulmones, el hígado y el esqueleto. Se recomienda una tomografía computarizada de la pelvis, ampliada para detectar ganglios linfáticos, así como una ecografía del hígado, un examen de rayos X del tórax para buscar metástasis en el pulmón y hueso.
Se recomienda el examen físico, incluido el tacto rectal y la palpación pélvica bimanual, cuando se detecta una hematuria. Sin embargo, el 85 % de los pacientes con cáncer de vejiga presentan inicialmente un tumor superficial y no palpable. No obstante, la exploración física y antecedentes, incluido el control de signos de enfermedad, como masas o cualquier otra cosa que parezca anormal y la historia médica de las enfermedades y los tratamientos anteriores del paciente, desempeñan un papel importante en el diagnóstico del cáncer de vejiga y para descartar otras patologías concomitantes.
Los grandes tumores pueden verse como defectos de llenado de la vejiga o como una asimetría en la expansión de las paredes de la vejiga durante el llenado en tumores invasivos. La urografía intravenosa también se lleva a cabo para detectar defectos de llenado en los cálices, pelvis renal y uréteres e hidronefrosis que pueden indicar la presencia de cáncer urotelial o una invasión del músculo vesical en el meato ureteral. La necesidad de practicar rutinariamente una urografía intravenosa como método de diagnóstico inicial es cuestionada debido a la baja incidencia de obtener hallazgos importantes con esta técnica.
La ultrasonografía se utiliza cada vez con más frecuencia como prueba inicial de imagen del tracto urinario, no solo porque evita el uso de contrastes intravenosos a los que algunos pacientes pueden ser alérgicos, sino porque también los transductores son cada vez más sensibles y permiten mejorar las imágenes del tracto urinario superior y vejiga. La ecografía abdominal permite distinguir masas renales, hidronefrosis y visualizar defectos de llenado intraluminal en la vejiga. Combinada con la radiografía simple de abdomen, la ecografía puede ser más exacta para esclarecer la causa de la hematuria que la urografía intravenosa y demuestra estar más indicada para detectar tumores vesicales.
La tomografía axial computarizada TAC es una parte de la evaluación de los tumores de vejiga invasivos y de la evaluación de las metástasis de ganglios linfáticos pélvicos y abdominales. Es de utilidad en la predicción de la extensión local de la enfermedad visualizando el tejido perivesical, que puede ser anormal debido a procesos inflamatorios causados por resecciones transuretrales previas y que pueden conducir a un estadio superior. El TAC permite evaluar el aumento del tamaño de los ganglios linfáticos, pero no proporciona información sobre el aspecto microscópico de la enfermedad. Por eso, la sensibilidad en detectar metástasis ganglionares es baja. Sobre esta base, la mayor utilidad de la TAC está relegada a la detección de adenomegalias y posibles metástasis hepáticas.
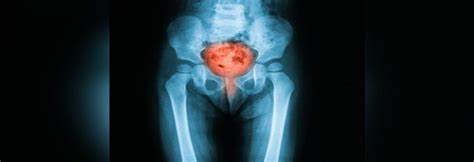
La importancia clínica de realizar una gammagrafía ósea de rutina antes de la cistectomía radical en los tumores de vejiga infiltrantes es cuestionable, excepto en presencia de una elevación del nivel de fosfatasa alcalina o en pacientes que presentan dolor de huesos.
Se debe obtener un urinocultivo y un sedimento urinario que descarten otras patologías como una infección urinaria. La visualizadión de células malignas en la orina es muy útil en presencia de un carcinoma in situ de alto grado de malignidad. Las muestras para la citología deben obtenerse cuando el paciente esté bien hidratado para optimizar la visualización de células cancerosas. Las muestras de orina para citología no deben obtenerse de la primera orina de la mañana. Incluso si los estudios de imagen del tracto urinario superior o vejiga son negativos, los hallazgos de una citología urinaria positiva pueden indicar una fuente de cáncer en cualquier localización del tracto urinario, en los cálices renales, a lo largo de los uréteres, en la vejiga y en la uretra.
Más aún, una citología urinaria negativa no excluye necesariamente la presencia de un cáncer de vejiga de bajo grado. La interpretación citológica puede ser problemática por baja recogida de células, atipias, cambios degenerativos y alteraciones terapéuticas que contribuyen a aumentar la dificultad. Estos argumentos estimulan la investigación de pruebas más fiables de orina para detectar cánceres uroteliales.
Se han realizado muchos estudios para evaluar marcadores urinarios. Las pruebas de antígenotumoral vesical, NMP22 (Nuclear Matrix Protein) productos de la degradación de la fibrina y otros están disponibles comercialmente. Muchas de estas pruebas tienen una mayor sensibilidad en detectar cáncer de vejiga, pero la especificidad es mucho más baja. Por tanto, los falsos positivos pueden llevar a la realización de innecesarias pruebas de imagen o biopsias de vejiga. No queda claro, pues, si estas pruebas proporcionan una información añadida con la que se puedan tomar decisiones útiles de tratamiento y pronóstico de los tumores superficiales de vejiga por la ausencia de datos que ofrecen los estudios prospectivos multicéntricos. Combinando estos nuevos marcadores se puede optimizar su rendimiento, aportando las ventajas de unas pruebas para corregir los inconvenientes de las otras. Hasta que no existan datos concluyentes sobre el beneficio de los nuevos marcadores o se encuentren otros mejores, la citología urinaria seguirá siendo la prueba principal para detectar cáncer de vejiga.
El diagnóstico del cáncer de vejiga depende en última instancia del examen cistoscópico de la vejiga y de la evaluación patológica de las lesiones resecadas. La cistoscopia proporciona información del tamaño, localización y apariencia del tumor dentro de la vejiga. Estas observaciones cistoscópicas, además de describirse por escrito, deben dibujarse en un esquema o almacenarse en formato de foto o vídeo. La cistoscopia puede practicarse inicialmente sin anestesia cuando se quiera valorar un paciente con cáncer de vejiga. Si un cáncer de vejiga ha sido detectado precozmente en pruebas de imagen o si una citología urinaria ha sido previamente positiva, el diagnóstico cistoscópico puede ser omitido y el paciente puede ser programado para efectuar una cistoscopia y biopsia o resección tumoral bajo anestesia. Se extirpa una porción del tejido o toda el área que preocupa y se envía al laboratorio para su análisis. Con el paciente anestesiado debe realizarse una exploración bimanual, primero para valorar la presencia de una masa palpable en la vejiga y, si existe, valorar su fijación a la pared pélvica. El examen bimanual puede ser realizado antes o después de la resección transuretral.
La presencia de una masa palpable tras la resección implica la existencia de un tumor extravesical. Puede ser de un interés particular en el seguimiento del resultado de la irradiación precistectomía. La RTU del cáncer de vejiga debe realizarse con la máxima preservación de la arquitectura y de las relaciones del tumor con las capas de la pared vesical. La extensión con la que el tumor invade las diferentes capas de la pared vesical ha sido de siempre usado inicialmente para estadiar el cáncer de vejiga y determinar el pronóstico. Para una evaluación patológica, los componentes más superficiales del tumor deben ser resecados separadamente de los componentes más profundos. Debe usarse lo menos posible la cauterización eléctrica, con el fin de preservar los detalles patológicos y evitar artefactos de la cauterización. Las muestras de biopsia del tumor y las de áreas sospechosas deben obtenerse de toda la extensión de la enfermedad. Se deben realizar tanto biopsias frías en sacabocados para preservar la arquitectura histológica como biopsias obtenidas de la RTU para determinar la extensión de la enfermedad. Las biopsias aleatorias de mucosa normal están indicadas ante una citología positiva, incluso en ausencia de tumor o ante cualquier tumor no papilar. Las biopsias al azar en pacientes con lesiones papilares solitarias están contraindicadas debido a que no aportan información adicional y porque pueden ser peligrosas, ya que las lesiones de la mucosa pueden provocar la implantación de células tumorales. Las biopsias de uretra prostática por RTU están indicadas ante la sospecha de un carcinoma in situ de vejiga, debido a la alta frecuencia de afectación de la uretra prostática.
Un método para reducir la recurrencia de tumores es el uso de medicación después de la resección transuretral (RTU). Los dos medicamentos más comunes que se usan para este propósito son el Bacilo Calmette-Guérin (BCG) y la mitomicina. Para las personas que ya se han sometido a una RTU, la BCG puede generar un riesgo similar de muerte y puede reducir el riesgo de recurrencia del tumor. Sin embargo, este medicamento puede aumentar el riesgo de efectos secundarios graves. Se necesita más investigación para confirmar estos resultados.
En caso de cáncer de vejiga que infiltra la capa muscular y está indicado un tratamiento radical hay que realizar:
El tratamiento del cáncer de vejiga depende de la profundidad con la que el tumor invade la pared de la vejiga. Las estrategias de tratamiento para el cáncer de vejiga incluyen:
El plan terapéutico para las lesiones Ta-T1 debe realizarse teniendo en cuenta el riesgo de la recurrencia y progresión de la enfermedad (factores pronóstico de los tumores), efectos secundarios y coste efectivo del tratamiento. La tasa de recurrencia de los carcinomas superficiales de vejiga (CSV), incluso después de un tratamiento adecuado, está bien documentado. El riesgo de progresión para transformarse en un cáncer invasivo es bajo en la mayoría de los casos, pero es mayor del 50% en los casos de alto grado T1G3, que representan cerca del 10% de los casos. El riesgo de enfermedad recurrente y de progresión puede predecirse basándose en los datos clínicos y patológicos, que proporcionan la RTU inicial y las pruebas diagnósticas del CSV. Existen unos factores pronóstico del CSV:
Una instilación vesical única con epirrubicina o mitomicina C dentro de las seis horas siguientes a una RTU es capaz de reducir la tasa de enfermedad recurrente cerca del 50 % y está por lo tanto indicada en todos los casos de CVS, excepto cuando se sospecha perforación vesical. La BCG está contraindicada debido al peligro de efectos secundarios sistémicos cuando existan heridas abiertas en la vejiga.
En los tumores de riesgo intermedio que necesitan más instilaciones, una instilación precoz puede requerir un tratamiento de mantenimiento. Una instilación inmediatamente después de la RTU con un agente quimioterápico debe ser realizado en todos los casos. Los tumores únicos, Ta-T1, G1, menores de 3 cm de diámetro, y los tumores papilares no necesitan tratamiento adicional porque la tasa de recaída en este grupo es muy baja, menos de 0,2 recaídas al año después de una instilación vesical única inmediatamente después de RTU.
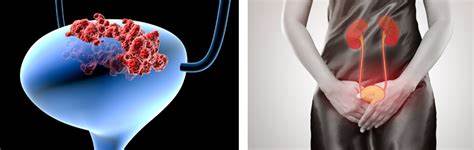
Los tumores no músculo invasivos no tratados pueden comenzar gradualmente a infiltrarse en la pared muscular de la vejiga (cáncer de vejiga músculo invasivo). Los tumores que se infiltran en la pared de la vejiga requieren una cirugía más radical, en la que se extrae una parte (cistectomía parcial) o toda (cistectomía radical) de la vejiga (una cistectomía) y el flujo urinario se desvía hacia un asa intestinal aislada (llamada conducto ileal o urostomía ). En algunos casos, los cirujanos pueden crear una vejiga sustituta (una neovejiga) a partir de un segmento de tejido intestinal, pero esto depende en gran medida de la preferencia de la persona, la edad de la persona, la función renal y el sitio de la enfermedad.
Una linfadenectomía pélvica bilateral debe acompañar a la cistectomía radical. Como mínimo, se debe seguir una plantilla estándar de linfadenectomía mediante la extirpación de los ganglios linfáticos ilíacos y obturadores externos e internos. Una linfadenectomía pélvica bilateral debe acompañar a la cistectomía radical. Como mínimo, se debe seguir una plantilla estándar de linfadenectomía mediante la extirpación de los ganglios linfáticos ilíacos y obturadores externos e internos. Al realizar una linfadenectomía, el cirujano puede extirpar los ganglios linfáticos de un área más pequeña (estándar) o de un área más grande (extendida). En comparación con una disección de ganglios linfáticos estándar, una disección prolongada puede reducir la probabilidad de muerte de una persona por cualquier motivo, incluida la muerte por cáncer de vejiga. El procedimiento prolongado puede producir efectos no deseados más graves y puede o no influir en la probabilidad de que el cáncer recurra con el tiempo. La tasa de efectos secundarios no tan graves sería similar para ambas cirugías.
El pembrolizumab probablemente mejore un poco la supervivencia general y puede mejorar levemente la calidad de vida de las personas con cáncer urotelial que ha empeorado después del tratamiento inicial en comparación con la quimioterapia continua. Sin embargo, el pembrolizumab podría tener solo efectos mínimos sobre la tasa de mortalidad o la tasa en la que avanza el cáncer. El pembrolizumab podría causar efectos secundarios menos graves que la quimioterapia.
Muchos grupos de investigadores clínicos en el campo del CSV han identificado factores que permiten identificar diferentes categorías pronósticas. Muchos parámetros importantes de los factores pronóstico se pueden obtener fácilmente. Para la enfermedad recurrente, los factores pronóstico en importancia decreciente son:
Basados en los factores pronóstico, el CSV puede dividirse en los siguientes grupos de riesgo:
En los pacientes con cáncer de vejiga en estadio II, el riesgo de morir por la enfermedad u otras causas aumenta si no se los opera dentro de las 12 semanas de realizado el diagnóstico.
Agregué información traducida de en:Bladder cancer
Escribe un comentario o lo que quieras sobre Cáncer de vejiga (directo, no tienes que registrarte)
Comentarios
(de más nuevos a más antiguos)
Aún no hay comentarios, ¡deja el primero!