Ruta del ácido shikímico
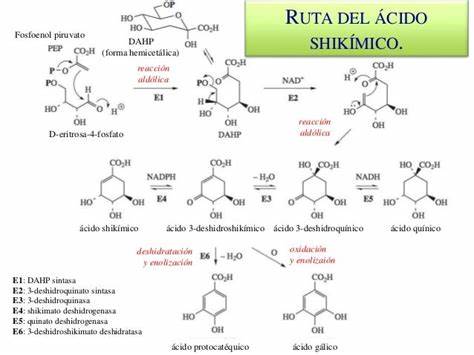
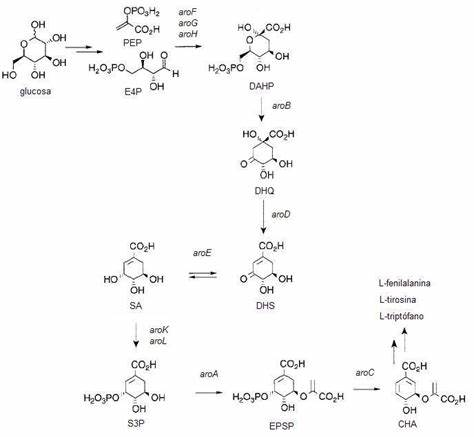
La ruta del ácido shikímico es un conjunto de reacciones metabólicas de gran relevancia en la biosíntesis de los tres aminoácidos proteínicos aromáticos fenilalanina, tirosina y triptófano, así como una extensa gama de metabolitos secundarios. El ácido shikímico es precursor de diversos intermediarios metabólicos aromáticos, tales como los taninos, el cloranfenicol, el ácido 4-aminobenzoico, los fenilpropanoides, los lignanos, los aminoácidos aromáticos, así como sus derivados: glucósidos cianogénicos aromáticos, aminas biógenas aromáticas, catecolaminas, betalaínas, melaninas, bisindoles, los flavonoides, las fenazinas y diversos alcaloides entre los cuales se encuentran los alcaloides tetrahidroisoquinolínicos, los alcaloides del ergot y los morfinanos, entre otros. El intermediario principal es el ácido shikímico, un compuesto originalmente aislado de plantas del género Illicium. En compuestos aromáticos derivados del ácido shikímico, las posiciones oxigenadas son de tipo catecol (orto) o pirogalol (diorto), y en el caso de los fenoles monooxigenados son generalmente p-hidroxi-compuestos.
Esta ruta es empleada por bacterias, algas, plantas y algunos hongos pero no por animales y protozoarios. Sin embargo, los tres aminoácidos aromáticos son esenciales para la vida.
El ácido shikímico se puede dividir en las siguientes secciones:
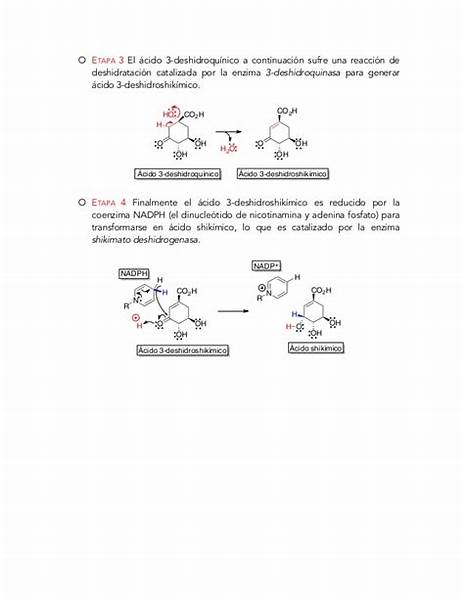
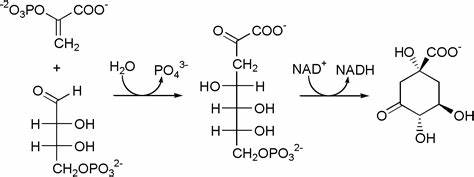
El ácido shikímico se biosintetiza originalmente del fosfoenol piruvato y la eritrosa 4-fosfato para formar el precursor denominado ácido 3-deshidroquínico. Este ácido puede formar varios metabolitos, como el ácido gálico, el ácido protocatequico, el ácido quínico y el ácido shikímico:
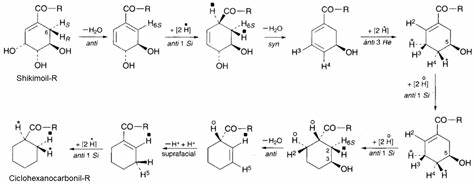
Mientras que el ácido gálico representa uno de los derivados más oxidados del ácido shikímico, por otra parte se tiene uno de los derivados más reducidos, el ácido ciclohexanocarboxílico. Es raro encontrarlo libre: más bien funge como residuo estructural de metabolitos más complejos, por ejemplo antibióticos como la ansatrienina, las trienomicinas, las tiazinotrienomicinas, la asukamicina y en los ácidos grasos ω-ciclohexílicos de ciertas bacterias termófilas y mesófilas (como Alicyclobacillus), por ejemplo el ácido ω-ciclohexilundecanoico. Fleet y colaboradores elucidaron los pasos de reducción del ácido shikímico hasta el éster del ácido ciclohexanoico:

Existen bacterias que han modificado la ruta de biosíntesis del shikimato de manera que se obtiene un derivado similar al ácido gálico pero con distintos patrones de grupos funcionales. Un ejemplo interesante es la biosíntesis del ácido 3-amino-5-hidroxibenzoico (AHBA). Específicamente, la biosíntesis comienza con la adición del fosfoenolpiruvato (PEP) a la eritrosa-4-fosfato. Al producto formado se adiciona una molécula de amoniaco para dar el ácido 4-amino-3-desoxi-D-arabino heptulosónico-7-fosfato (aminoDHAP). Después, la DHQ sintasa cataliza el cierre de un anillo para producir el ácido 4-amino-3-deshidroquínico (aminoDHQ). El producto sufre una doble oxidación vía aminoDHQ deshidratasa para dar el 4-amino-deshidroshikimato (aminoDHS). El intermediario clave, el ácido 3-amino-5-hidroxibenzoico (AHBA), se forma por aromatización de la AHBA.
El AHBA es precursor de en las biosíntesis de todas las mitomicinas procede por combinación de ácido 3-amino-5-hidroxibenzoico(AHBA), D-glucosamina (aparece mal representada abajo), y fosfato de carbamilo, y así se forma el anillo de mitosano. El núcleo de mitosano es sintetizado via condensación entre AHBA y D-glucosamina. Una vez que la condensación ha ocurrido, el mitosano sufre interconversiones de grupos funcionales.
El AHBA también es precursor de otros productos naturales anticáncer tales como la rifamicina y la ansamicina.
El ácido shikímico puede producir por una vía enzimática de 3 pasos uno de los metabolitos intermedios más importantes de la ruta del ácido shikímico, el ácido corísmico:
En esta ruta se llevan a cabo 3 reacciones:
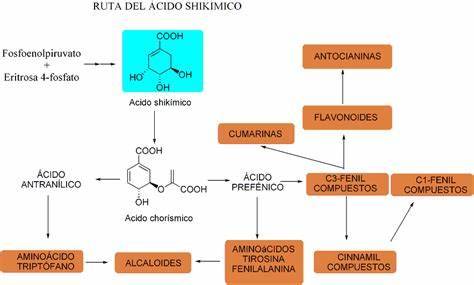
El ácido corísmico puede producir metabolitos de gran diversidad bioquímica:
Las filoquinonas (vitamina K1) y las menaquinonas (vitamina K2) son derivados de la naftoquinona derivados del shikimato que se encuentran en plantas y algas (vitamina K1) o bacterias y hongos (vitamina K2). La estructura de filoquinona más común tiene una cadena lateral diterpenoide, mientras que el rango de estructuras de menaquinona tiende a ser bastante más amplio con 1-13 unidades de isopreno. Estas quinonas se derivan del ácido isocorísmico y de un precursor adicional con 4 carbonos proporcionados por el ácido 2-oxoglutárico, que se incorpora mediante un mecanismo que implica la coenzima tiamina difosfato (TPP), de manera análoga a la piruvato descarboxilasa. El ácido 2-oxoglutárico se descarboxila en presencia de TPP para dar el anión TPP de semialdehído succínico, que ataca al ácido isocorísmico en una reacción de tipo Michael. La pérdida del cofactor de tiamina, la eliminación del ácido pirúvico y luego la deshidratación producen el ácido o-succinilbenzoico intermedio (OSB). Esto se activa por la formación de un éster de coenzima A, y una condensación similar a Dieckmann permite la formación de anillos. El ácido 1,4-dihidroxinaftoico es el tautómero aromático más favorecido de la hidrólisis del éster de la coenzima A.
La OSB y el ácido 1,4-dihidroxinaftoico, o su tautómero diceto, se ven implicados en la biosíntesis de una amplia gama de naftoquinonas y antraquinonas vegetales.. Hay paralelismos con las últimas etapas de la secuencia de la menaquinonas, o diferencias de acuerdo con la especie de la planta en cuestión. Se encuentra que la sustitución de la función carboxilo por un sustituyente isoprenilo transcurre a través de un intermedio disustituido en plantas del género Catalpa (Fam. Bignoniaceae) y Streptocarpus (Fam. Gesneriaceae), como la catalponona, y esta puede transformarse en lapachol. La lawsona y la juglona se forman por secuencias oxidativas en la que para la laysona el hidroxilo reemplaza al carboxilo, mientras que en la juglona la descarboxilación, insaturación e hidroxilación parecen ser independientes. Otra ruta hipotética es la síntesis de un esqueleto de antraquinona ciclando de forma oxidativa (quizás radicalaria) a un sustituyente dimetilalilo en el sistema de naftaquinona.
El ácido 1,4-dihidroxinaftoico es ahora el sustrato para la alquilación y la metilación como se ve con ubiquinonas y plastoquinonas. Sin embargo, se encuentra que el fragmento terpenoide reemplaza al grupo carboxilo, y el análogo descarboxilado no está involucrado. La transformación del ácido 1,4-dihidroxinaftoico en naftoquinona isoprenilada parece estar catalizada por un único enzima. Esto implica la alquilación, la descarboxilación del β-cetoácido resultante, y finalmente una oxidación a la p-quinona.
Las rutas de los aminoácidos aromáticos L-fenilalanina y L-tirosina a partir del ácido prefénico pueden variar de acuerdo al organismo, y en muchos casos puede operar más de una ruta en una especie. En esencia, tres tipos de reacción están implicadas: Transaminación, aromatización descarboxilativa e hidroxilaciones, pero lo que cambia en los organismos es el orden en el que se llevan a cabo. Así, en algunos organismos se pueden producir tanto sustratos del ácido arogénico como del prefénico. Muchas bacterias y plantas tienden a sintetizar la fenilalanina y la tirosina por separado.
Los animales, en cambio, carecen de la ruta del ácido shikímico, por lo que la fenilalanina resulta esencial, no así la tirosina, la cual se puede obtener por la para-hidroxilación de la fenilalanina:

La L-fenilalanina y la L-tirosina son bloques de construcción para una amplia gama de metabolitos secundarios: los fenilpropanoides (Compuestos tipo C6C3). En plantas, el primer paso es la eliminación del nitrógeno de la fenilalanina en forma de amoniaco para generar el ácido trans-cinámico (En el caso de la tirosina se forma Ácido p-coumárico) Todas las plantas pueden desaminar fenilalanina por medio de la fenilalanina amoniaco liasa (PAL), pero la desaminación de tirosina parece ser más restringida a miembros de la familia Poaceae. La tirosina amoniaco liasa (TAL) ha sido encontrada en plantas y bacterias. Aquellos organismos que no pueden desaminar la tirosina obtienen el ácido p-coumárico por hidroxilación del ácido cinámico.
Los arilpropanoides pueden formar tioésteres de arilpropionil coenzima A y trasferirse a diversos sustituyentes hidroxilo de aminoácidos (Ser, Thr), mononosacáridos o compuestos fenólicos.
La degradación por β-oxidación¨ de los arilacrilatos y sus derivados de reducción (alcoholes y aldehídos) se pueden degradar para perder dos unidades de carbono y formar así derivados toluenos, formilfenoles y ácidos hidroxibenzoicos simples u O-metilados.
Existen casos en donde hay una segunda condensación tipo aciloínica con tiamina para formar nuevos arilpropanoides con distinto patrón de grupos funcionales denominados efedrinas:
La novobiocina, también conocida como albamicina o catomicina, es un antibiótico tipo aminocumarina producido por la bacteria Streptomyces niveus ,que recientemente ha sido identificado como un sinónimo subjetivo de S. spheroides, un miembro de la orden de las actinobacterias o actinomycetes. Otros antibióticos de la clase de las aminocumarinas son la clorobiocina y la cumermicina A1.
Se ha encontrado que los seres vivos pueden catabolizar la tirosina, la fenilalanina y los fenilpropanoides a esqueletos aromáticos con una cadena lateral de dos carbonos. La L-fenilalanina puede degradarse por descarboxilación (con catálisis de la Descarboxilasa de los aminoácidos aromáticos, EC 4.1.1.28) para producir feniletilamina, o por transaminación para dar el ácido fenilpirúvico.
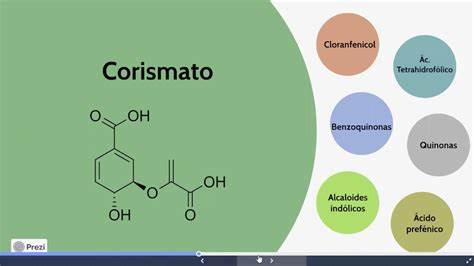
La fenetilamina puede transaminarse para dar el fenilacetaldehído. Este compuesto se oxida a ácido fenilacético por acción de una aldehído deshidrogenasa (EC 1.2.1.5). Posteriormente una monooxigenasa hidroxila el anillo aromático en posición meta. Una vez más, se puede hidroxilar por la acción otra monooxigenasa en la posición 4. El producto intermediario es el ácido homoprotocatecuico. El ácido fenilacético se puede esterificar con la Coenzima A.
Por otro lado, el ácido fenilpirúvico sufre una descarboxilación oxidativa para formar fenilacetaldehído, el cual se puede incorporar a la ruta anteriormente descrita.
De modo análogo, la tirosina puede descarboxilarse o transaminarse, como se indicó en el inciso anterior. El producto de transaminación (Ácido p-hidroxifenilpirúvico) puede ser epoxidado en la posición 1,2 con transposición para dar el ácido homogentísico. Si el producto de transaminación se descarboxila con oxidación, se forma el 4-hidroxifenilacetaldehído. El producto de descarboxilación de la tirosina (la tiramina) al transaminarse forma también el 4-hidroxifenilacetaldehído. Este compuesto se oxida a su correspondiente ácido carboxílico, el cual se puede oxigenar por acción de la 4-hidroxifenilacetato 1-monooxigenasa (EC 1.14.13.18). El producto por acción de esta enzima produce también ácido homogentísico. Otra ruta que puede tomar el ácido 4-hidroxifenilacético es oxigenarse por acción de otra enzima, la 4-hidroxifenilacetato-3-monooxigenasa de cadena larga (EC 1.14.14.9). El producto de esta reacción es el ácido homoprotocatecuico.
La degradación de los aminoácidos tirosina y fenilalanina puede producir, dependiendo el organismo, 3 compuestos intermediarios:
Cada uno de estos intermediarios tiene distintas formas de catabolizarse, lo cual deja ver la gran diversidad metabólica que existe en los seres vivos para el aprovechamiento energético de varios compuestos aromáticos.
La 3,4-dihidroxifenilalanina (DOPA) es un precursor relevante en el metabolismo de la tirosina y la fenilalanina. Se produce por la hidroxilación de la tirosina y produce varios metabolitos secundarios tales como las melaninas, las catecolaminas, las betalaínas, las higroaurinas, los alcaloides tetrahidroisoquinolínicos y otros alcaloides.
La adrenalina es una hormona que es sintetizada en la médula de la glándula suprarrenal en una ruta enzimática que convierte el aminoácido tirosina en una serie de intermediarios y, finalmente, en adrenalina. La tirosina es primero oxidada para obtener levodopa, que posteriormente se descarboxila para dar dopamina. La oxidación de esta molécula proporciona norepinefrina que luego es metilada para dar epinefrina. También que es sintetizada al metilarse la amina distal primaria de la norepinefrina por la acción de la enzima feniletanolamina N-metiltransferasa (PNMT) en el citosol de las neuronas adrenérgicas y células de la médula adrenal (llamadas células cromafínicas). La PNMT solo se encuentra en el citosol de las células de la médula suprarrenal. La PNMT usa la S-adenosilmetionina como cofactor para donar el grupo metilo a la norepinefrina, formando así la adrenalina.
La función estabilizadora de membrana de los ácidos grasos ω-ciclohexílicos de varias especies de Alicyclobacillus se reemplaza de manera única en una especie, A. cycloheptanicus, por los ácidos grasos homólogos, los ácidos grasos ω-cicloheptílicos. El espectro de ácidos grasos encontrados es similar a aquel de los ácidos grasos de ciclohexilo en las otras especies de Alicyclobacillus, excepto por la presencia de un cicloheptano en lugar del ciclohexano. Esto plantea la intrigante cuestión de si la equivalencia funcional de los dos tipos de compuestos es el resultado de una biosíntesis divergente o convergente. Cane y colaboradores reportaron la biosíntesis de tiotropocina, un metabolito de una especie de Pseudomonas que contiene un esqueleto de carbono idéntico al del ácido cicloheptanocarboxílico. Cane y colaboradores conclyeron con estudios de marcaje isotópico que el esqueleto cicloheptánico de la roseobacticida, las tropolonas bacterianas y los ácidos ω-cicloheptílicos surgen de la expansión del anillo de un éster de ácido fenilacético derivado de la fenilalanina.
En muchos casos se lleva a cabo una segunda ciclización, en la que se forma un compuesto policíclico. La aranotina presenta adicionalmente una electrociclización reversa a partir del epóxido de areno correspondiente para forma r un sistema de oxepina.
Químicamente son sustancias polifenólicas, relacionadas con el metabolismo de la fenilalanina a través de la dimerización de alcoholes cinámicos (principalmente el alcohol coniferílico) sustituidos (ver Ácido cinámico) a un esqueleto de dibencilbutano 2. Esta reacción es catalizada por enzimas oxidativas y normalmente es controlada por proteínas de dirección. La estructura básica de estas sustancias son dos unidades C
6C
3 unidas por enlaces β,β' utilizadas para la nomenclatura de los lignanos.
La biosíntesis de lignanos más estudiada es la ruta de la podofilotoxina:
La polimerización no selectiva de los derivados del alcohol coniferílico forma la lignina, un biomaterial de aspecto pétreo. Las ligninas son particularmente importantes en la formación de las paredes celulares, especialmente en la madera y la corteza, ya que prestan rigidez y no se pudren fácilmente.
Por otro lado, existen microorganismos que producen enzimas modificadoras de la lignina (LMEs) que catalizan la descomposición de la lignina. No son hidrolasas, sino peroxidasas, como la lignina peroxidasa (EC 1.11.1.14), la manganeso peroxidasa (EC 1.11.1.13), la peroxidasa genérica (EC 1.11.1.16) y muchas fenoloxidasas del tipo lacasas. Los organismos más estudiados que producen estas enzimas son los hongos Phanerochaete chrysosporium, Ceriporiopsis subvermispora, Trametes versicolor, Phlebia radiata, Pleurotus ostreatus y Pleurotus eryngii. Los organismos productores de estas enzimas son cruciales para los ciclos ecológicos (por ejemplo, crecimiento / muerte / descomposición / rebrote, ciclo del carbono y restauración del suelo) porque permiten que el tejido vegetal se descomponga rápidamente, liberando la materia orgánica para su reutilización en las nuevas generaciones de vida.
Las unidades de hidroxicinamoil-CoA, hidroxiarilacetil-CoA o hidroxibenzoil-CoA pueden incorporarse como unidades de iniciación en ácido graso sintasas (FAS) o policétido sintasas (PKS). Se forman ácidos ω-arilcarboxílicos grasos, n-alquilfenoles o arilpolicétidos, los cuales ciclizan para formar un segundo anillo fenólico pero con un patrón alternado de hidroxilación, distinto al de la ruta de los fenilpropanoides. Así se forman las xantonas, los dibenzofuranoides, los estilbenos y las chalconas. Estos compuestos, adicionalmente pueden acoplarse, metilarse, glicosilarse, o prenilarse en los anillos, dando así todavía una mayor diversidad en estos compuestos. Un ejemplo de estilbeno policíclico de hepáticas es la cavicularina.
A su vez, las chalconas forman uno de los grupos fitoquímicos más extendidos y representativos en las plantas angiospermas: los flavonoides. Estos compuestos, adicionalmente pueden acoplarse, metilarse, glicosilarse, o prenilarse en los anillos, dando así todavía una mayor diversidad en estos compuestos. Las 'auronas producen un cierre furanoide (en lugar del piranoide de los flavonoides) y se encuentran restringidas taxonómicamente.
Los isoflavonoides se forman por migración radicalaria del fenilo de la posición 2 a la 3.
Las catequinas son flavonoides reducidos en el anillo piranoide que polimerizan por radicales libres entre los anillos aromáticos fenólicos y los piranoides de la otra unidad, entre dos y quince unidades. A estos compuestos se les denomina taninos condensados.
Los taninos condensados son los pigmentos principales de muchas semillas, y también están presentes en los tejidos vegetativos de algunas plantas forrajeras. Como todos los taninos, aparentemente en las plantas cumplen funciones de defensa ante el herbivorismo. Son de importancia económica para el ganado porque reducen la hinchazón en los animales rumiantes, pero al mismo tiempo tienen potencial de producir rechazo al alimento ("antialimentarios") y de disminuir la absorción de los nutrientes por el organismo ("antinutrientes").
Los productos de transaminación de aminoácidos aromáticos son el ácido fenilpirúvico y el ácido p-hidroxifenilpirúvico, los cuales pueden ser interconvertibles en algunos organismos via prefenato. El ácido fenilpirúvico puede reducirse para formar ácido 3-fenil láctico, el cual puede transformarse por transposición en ácido trópico, componente de la hiosciamina. El ácido fenilpirúvico puede dimerizarse por medio de una condensación aldólica doble para formar ácido polipórico, el cual es precursor de varios terfenilos, por ejemplo atromentina, volucrisporina, leucomelona, muscafurina, ácido telefórico y xileritrina.
El ácido polipórico puede escindirse oxidativamente para formar ácido pulvínico y sus derivados. El ácido 4-hidroxifenilpirúvico es precursor de la 4-hidroxifenilglicina, aminoácido componente de péptidos no ribosomales, como en el caso de la vancomicina.
El ácido homogentísico es un catabolito de la tirosina precursor de los tocoferoles, ubiquinonas y ácido hiposudórico:

La melanina es un pigmento que se produce en los animales. La forma más común de melanina es la eumelanina, un polímero negro-marrón de ácidos carboxílicos de dihidroxindol y sus formas reducidas. El proceso de formación de la melanina (melanogénesis), es estimulada por el daño en el ADN inducido por la radiación ultravioleta. La eumelanina y la feomelanina se producen en el estrato más profundo de la epidermis (estrato basal) y en las células de la matriz del folículo pilosebáceo.
Las betaxantinas son betalainas que consisten en bases de Schiff del ácido betalámico con un aminoácido, mientras de que en las betaninas contienen un catión iminio con cicloDOPA.
Muchos taxones de Amarilidáceas son conocidos por su extremada toxicidad. La familia Amaryllidaceae produce un grupo de alcaloides cuyo precursor es la norbeladina, una amina formada por la reducción de la base de Schiff formada entre el aldehído protocatecuico y la tiramina. La norbeladina puede acoplar por radicales libres los dos anillos aromáticos que presenta. Así, pueden formarse distintas estructuras de acuerdo al patrón de acoplamiento de los anillos. Ejemplos: Norbeladina, criptostilina I, cherilina, y nivalidina, galantamina, hemantidina, tazetina, y pancracina. Montanina. Licorina, Licorenina. Narciclasina. Principalmente se tienen los esqueletos tipo Licorina, Crinina y Galantamina.
Los alcaloides isoquinolínicos y tetrahidroisoquinolínicos (THIQ) comprenden una diversa gama de compuestos ampliamente distribuidos principalmente en el reino vegetal. Cabe destacar que estas isoquinolinas tienen un sustituyente alquilo en la posición 1. Cualquier otro patrón de sustitución hace pensar en otra ruta biosintética. Biogenéticamente se pueden formar por una Reacción de Pictet-Spengler de una catecolamina con un aldehído o un ácido α-cetocarboxílico:
De acuerdo al aldehído utilizado, se pueden reconocer 4 grandes familias de este tipo de alcaloides:
Los alcaloides fenetilisoquinolínicos se forman en diversas monocotiledóneas. El derivado más conocido por sus propiedades farmacológicas contra la gota es la colchicina, una benzooctalenamina N acetilada aislada de Colchicum autumnale:
La emetina es un alcaloide de la ipecacuana que se forma por la ciclización tipo Pictet-Spengler con el secoiridoide denominado secologanina:

La aaptamina es un caso de un alcaloide isoquinolínico aislado de esponjas y que presenta un tercer anillo fusionado. De acuerdo a la hipótesis de Claridge, el esqueleto de la aaptamina se puede derivar de la S-3(3,4-dihidroxifenil)alanina(L-DOPA) y un equivalente biosintético del aldehído de la β-alanina, con los cuales se lleva a cabo la reacción de Mannich (en una reacción tipo Pictet-Spengler) para formar el equivalente de tetrahidroisoquinolina y con heterociclización sobre el anillo de benceno de la quinolina. Posteriormente se lleva a cabo una descarboxilación y deshidrogenación para producir la 8,9-bisdesmetilaaptamina. Este compuesto, por metilaciones posteriores produce la aaptamina.
La salinosporamida A (Marizomib) es un potente inhibidor del proteasoma que se estudia como posible agente anticanceroso. Ingresó en la fase I de ensayos clínicos en humanos para el tratamiento del mieloma múltiple, solo tres años después de su descubrimiento en 2003. Este producto marino natural es producido por las bacterias marinas obligadas Salinispora tropica y Salinispora arenicola, que se encuentran en los sedimentos oceánicos. La salinosporamida A pertenece a una familia de compuestos, conocidos colectivamente como salinosporamidas, que poseen un núcleo bicíclico de γ-lactama-β-lactona densamente funcionalizado.
Las plantas del género Securinega producen alcaloides con el esqueleto base (6S,11bS)-6,11b-metano-3a,6,11a,11b-tetrahidrofuro[2,3-c]pirido[1,2-a]azepina. Este pequeño grupo de 30 alcaloides parece provenir biosintéticamente de la tirosina y la lisina, como el caso de la securinina, un alcaloide aislado a partir de las hojas, raíces y tallos Securinega suffruticosa y Phyllanthus discoides(Euphorbiaceae).
Otros ejemplos son las securiniaminas, sufruticodina y los securinoles A-D. La filantidina tiene la estructura metanofuro[2,3-d]pirido[1,2-b][1,2]oxazocina.
El ácido antranílico es precursor de varios metabolitos secundarios por condensación o conjugación con moléculas provenientes de otras rutas.
La divulgación de las propiedades antimicrobianas de la murrayanina (3-formil-1-metoxicarbazol), aislado de la planta Murraya koenigii despertó un fuerte interés de los químicos y biólogos. Los alcaloides carbazólicos de plantas tienen como precursor al 3-metilcarbazol, el cual procede de la prenilación de la 4-hidroxiquinolona.
Estos alcaloides son indicadores quimiotaxonómicos de plantas pertenecientes a la familia Rutaceae (géneros: Murraya, Clausena, Glycosmis)
El triptófano se biosintetiza en tres etapas fundamentales: Unión entre el ácido antranílico y un éster fosfórico de ribosa con ciclización descarboxilativa, la eliminación de una molécula de gliceraldehído 3-fosfato, y la condensación con una molécula de serina. Durante la biosíntesis del triptófano, participan 4 enzimas:
Durante la biosíntesis del triptófano, existen unos cuantos metabolitos que proceden de intermediarios del triptófano y no de éste directamente. Por ejemplo, El DIMBOA (2,4-dihidroxi-7-metoxi-1,4-benzoxazin-3-ona) es un ácido hidroxámico heterocíclico con esqueleto tipo benzoxazinoide que se forma por oxidación tipo Baeyer-Villiger del intermediario en la biosíntesis del triptófano, el indol-3-glicerol-fosfato. El DIMBOA es una fitoalexina presente en el maíz y otras poáceas particularmente el trigo. En el maíz, el DIMBOA funciona como defensa natural contra insectos herbívoros como el lepidóptero taladro del maíz (Ostrinia nubilalis) y muchas otras plagas nocivas, incluyendo hongos y bacterias. El nivel exacto de DIMBOA varía entre plantas individuales, pero las concentraciones más altas son típicamente encontradas en plantas germinales y la concentración disminuye conforme a la edad de la planta:
El triptófano puede presentar reacciones adicionales que no alteran el esqueleto pero sí modifican el patrón de grupos funcionales. Las más comunes son:
La transformaciones estructurales más representativas (mas no las únicas) del triptófano y sus derivados son:
El esqueleto propanoide lateral al sistema indólico puede presentar degradaciones de acuerdo a los siguientes patrones bioquímicos:
Los hongos pueden formar anhidropéptidos dicetopiperazidínicos con en triptófano y otro aminoácido. Por ejemplo, en el caso del verruculógeno, una micotoxina producida por ciertas cepas de Aspergillus. Es un análogo anulado de ciclo (L-Trp-L-Pro) que pertenece a la clase más abundante y estructuralmente diversa de productos naturales de triptófano-prolina 2,5-dicetopiperazina. Produce temblores en ratones debido a sus propiedades neurotóxicas.
Cuando procede la Reacción de Pictet-Spengler con la triptamina, se forman alcaloides β-carbolínicos. Los compuestos carbonílicos condensados con triptamina más comunes son el ácido pirúvico, el cual forma 1-metil β-carbolinas (como la harmina) o aldehídos como la secologanina.
La estrictosidina es la precursora de distintos alcaloides con modificaciones estructurales y formación de intrincados compuestos policíclicos característicos de plantas del orden Gentianales. Se pueden distinguir diversas rutas como la del corinanteal, de la cual surge la quinina; la deshidrogeisosquizina, de la cual se diversifica a la prekuamicina y la catenamina, de donde provienen los yohimbinoides y la ajmalicina.
Un derivado de la prekuamicina, la estemadenina, puede formar distintos alcaloides tales como la elipticina:
La prekuamicina también es precursora de los sistemas tipo andranginina:
La secodina sufre ciclizaciones posteriores para formar los alcaloides tipo Cataranthus. Un metabolito particularmente estudiado de esta ruta es la vinblastina:
Las manzaminas son alcaloides β-carbolínicos producidos por una reacción tipo Mannich entre el triptófano y los ircinales A o B con posterior oxidación
La ciclización intramolecular del nitrógeno de la triptamina a la posición 2 del indol por metilación de la posición 3 forma los alcaloides pirroloindólicos, tales como la fisostigmina:
Los alcaloides del cornezuelo de centeno pueden considerarse derivados del compuesto tetracíclico 6-metilergolina. Los alcaloides naturales contienen un sustituyente en la configuración beta en la posición 8 y una unión doble en el anillo D. Los alcaloides de interés terapéutico son derivados amídicos del Ácido lisérgico; estos compuestos tienen una doble unión entre el carbono 9 y el carbono 10, y por esa razón pertenecen a la familia de los compuestos 9-ergoleno. Muchos alcaloides que contienen un grupo metilo o hidroximetilo en laposición 8 están presentes en el cornezuelo en cantidades mínimas. Se les denomina alcaloides de clavina y consisten primordialmente en 9-ergolenos (lisergol) y 8-ergolenos (elimoclavina, el isómero 8-ergoleno del lisergol). El triptófano puede ser prenilado en el anillo aromático por una reacción enzimática tipo Friedel-Crafts.
Este triptófano prenilado puede oxidarse para formar un anillo de seis miembros adicional fusionado, como en la chanoclavina I.La chanoclavina da una heterociclización para formar un anillo adicional de piperidina fusionada al de la chanoclavina, por ejemplo, la agroclavina. La oxidación del metilo terminal de la agroclavina forma el ácido lisérgico, uno de los alcaloides del ergot más conocidos:
El ácido lisérgico puede incorporarse a una polipéptido sintasa no ribosomal para formar alcaloides más complejos, como la β-ergocriptina.
Los alcaloides del cornezuelo de centeno son el primer grupo de fármacos de bloqueo adrenérgico que se descubrieron y su farmacología general se describió en estudios clásicos. Estos alcaloides del cornezuelo manifiestan una variedad compleja de propiedades farmacológicas. En grados variables, los agentes mencionados actúan como agonistas o antagonistas parciales a nivel de receptores α, receptores dopamínicos y de serotonina.
El triptófano puede incorporarse también a sistemas tipo policétido sintasa, como en el caso de las quetoglobosinas:
La dimerización del triptófano, analógica a la biosíntesis de los lignanos en fenilpropanoides, produce a diferencia de los furolignanos, sistemas tipo diindolilpirroles, en donde el ácido cromopirrólico es el principal intermediario. La formación de un anillo aromático adicional produce un sistema indolopirrolocarbazólico. Los alcaloides más representativos son la rebecamicina y la estaurosporina. La principal actividad biológica de la estaurosporina es la inhibición de las proteínas quinasas a través de la inhibición de la unión del ATP a la quinasa. Esto se logra mediante la mayor afinidad de la estaurosporina por el sitio de unión a ATP en la quinasa. La estaurosporina es un inhibidor prototípico de la quinasa ATP competitiva ya que se une a muchas quinasas con alta afinidad, aunque con poca selectividad.
Kimmel y colaboradores elucidaron la biosíntesis de la violaceína. Este compuesto proviene de dos unidades derivadas del triptófano, las iminas del triptófano y del 5-hidroxitriptófano. Posteriormente se condensan estas moléculas y se forma un anillo de pirrol correspondiente al ácido protoviolaceínico. Éste se descarboxila por oxidación para formar la violaceína.
El ácido quinurénico es un alcaloide quinolínico que se forma a partir de un catabolito del triptófano, la quinurenina. Cuando este aminoácido se transamina por la acción de la quinurenina—oxoglutarato transaminasa (EC 2.6.1.7), el grupo ceto forma una imina con el nitrógeno residual del anillo de indol del triptófano precursor. Cuando la cetona tautomeriza a enol, se finaliza así la formación del anillo de quinolina.
La orellanina es un metabolito secundario de la ruta del ácido shikímico, como derivado del ácido antranílico, ruta del catabolismo del triptófano, vía quinurenina. De la degradación de la quinurenina se obtiene el ácido 3-hidroxiantranílico
Se ha encontrado que los seres vivos pueden catabolizar la tirosina, la fenilalanina y los fenilpropanoides. La L-fenilalanina puede degradarse por descarboxilación (con catálisis de la Descarboxilasa de los aminoácidos aromáticos, EC 4.1.1.28) para producir feniletilamina, o por transaminación para dar el ácido fenilpirúvico.
La fenetilamina puede transaminarse para dar el fenilacetaldehído. Este compuesto se oxida a ácido fenilacético por acción de una aldehído deshidrogenasa (EC 1.2.1.5). Posteriormente una monooxigenasa hidroxila el anillo aromático en posición meta. Una vez más, se puede hidroxilar por la acción otra monooxigenasa en la posición 4. El producto intermediario es el ácido homoprotocatecuico. El ácido fenilacético se puede esterificar con la Coenzima A.
Por otro lado, el ácido fenilpirúvico sufre una descarboxilación oxidativa para formar fenilacetaldehído, el cual se puede incorporar a la ruta anteriormente descrita.
De modo análogo, la tirosina puede descarboxilarse o transaminarse, como se indicó en el inciso anterior. El producto de transaminación (Ácido p-hidroxifenilpirúvico) puede ser epoxidado en la posición 1,2 con transposición para dar el ácido homogentísico. Si el producto de transaminación se descarboxila con oxidación, se forma el 4-hidroxifenilacetaldehído. El producto de descarboxilación de la tirosina (la tiramina) al transaminarse forma también el 4-hidroxifenilacetaldehído. Este compuesto se oxida a su correspondiente ácido carboxílico, el cual se puede oxigenar por acción de la 4-hidroxifenilacetato 1-monooxigenasa (EC 1.14.13.18). El producto por acción de esta enzima produce también ácido homogentísico. Otra ruta que puede tomar el ácido 4-hidroxifenilacético es oxigenarse por acción de otra enzima, la 4-hidroxifenilacetato-3-monooxigenasa de cadena larga (EC 1.14.14.9). El producto de esta reacción es el ácido homoprotocatecuico.
La degradación de los aminoácidos tirosina y fenilalanina puede producir, dependiendo el organismo, 3 compuestos intermediarios:
Cada uno de estos intermediarios tiene distintas formas de catabolizarse, lo cual deja ver la gran diversidad metabólica que existe en los seres vivos para el aprovechamiento energético de varios compuestos aromáticos.
La degradación del ácido homoprotocatecuico procede por los siguientes pasos:
La fenilacetil-Coenzima A puede degradarse por dos vías:
La degradación del ácido homogentísico tiene dos posibles rutas:
El ácido benzoico es un metabolito de degradación de compuestos aromáticos en plantas y bacterias. Este compuesto es un xenobiótico que puede resultar tóxico para animales y hongos, por lo que los seres vivos han desarrollado distintas rutas complejas para la degradación del ácido benzoico o sus sales. El esquema general es la hidroxilación del ácido benzoico (la cual se puede efectuar en distintas posiciones) para dar intermediarios que pueden escindirse oxidativamente para dar derivados del ácido mucónico. Estos compuestos pueden seguirse oxidando para producir moléculas que pueden incorporarse en el ciclo de ácido cítrico:
Muchos mamíferos herbívoros eliminan el ácido benzoico por la formación del ácido hipúrico. La benzoil Coenzima A puede funcionar como unidad de iniciación en la ruta de los policétidos.
Escribe un comentario o lo que quieras sobre Ruta del ácido shikímico (directo, no tienes que registrarte)
Comentarios
(de más nuevos a más antiguos)
Aún no hay comentarios, ¡deja el primero!